El potencial germicida de determinadas longitudes de onda de la luz dentro del espectro electromagnético es una área de creciente interés, con las tecnologías basadas en el ultravioleta (UV) liderando este campo por su potencial virucida. Sin embargo, la fototoxicidad en humanos junto con la degradación de polímeros asociada a la radiación UV limitan su uso en espacios ocupados.
Como alternativa, se han ido explorando diferentes longitudes de onda más largas, con menos energía de irradiación, que pudieran sustituir a la UV para aplicaciones de desinfección. La luz visible de 405 nm, en el contexto de aplicaciones bactericidas y fungicidas es una posible alternativa.
La utilización de esta longitud de onda de luz visible está mediada por la absorción de las porfirinas dentro del organismo, creando especies reactivas de oxígeno que resultan en daños de radicales libres en su ADN y una interrupción de las funciones celulares. Sin embargo, el potencial virucida de las tecnologías basada en la luz visible han sido en gran medida inexplorados dada la falta de porfirinas en los virus.
Un nuevo estudio realizado por investigadores del Ichan School of Medicine at Mount Sinai y publicado en la “Scientific Reports” muestra el impacto de la irradiación de 405 nm en la inactivación de los virus SARS-CoV-2 y la gripe A H1N1 sin la mediación de fotosensibilizadores como las porfirinas.
“Dada la actual pandemia de COVID-19, queríamos explorar el impacto de la tecnología de luz visible enriquecida de 405 nm en la inactivación de patógenos respiratorios como el SARS-CoV-2 y el virus de la gripe A”, señalan los científicos en el paper.
Utilizando un sistema de desinfección de luz visible disponible comercialmente, los investigadores fueron capaces de garantizar que las dosis de irradiación fueran seguras y alcanzables en entornos clínicos reales. Los resultados apoyan el posible uso de la irradiación de 405 nm como una herramienta eficaz para la descontaminación continua de patógenos respiratorios como el SARS-CoV-2 y los virus de la gripe A.

UV-C vs Luz visible
Después de dos años de la aparición de la pandemia de COVID-19, la desinfección a través de radiación ultravioleta-C (UV-C) se ha posicionado como una herramienta muy útil para hacer frente a estas situaciones pandémicas. Se trata de una tecnología bien establecida y que ha demostrado que inactiva una gran gama de patógenos, incluyendo bacterias, hongos y virus.
El mecanismo de acción de la UV-C es la fotodimerización del material genético como el ARN (adecuado para el SARS-CoV-2) y el ADN (adecuado para los virus de ADN y patógenos bacterianos, entre otros). Desafortunadamente, este efecto se ha asociado con efectos nocivos en los humanos, como la fotoqueratoconjuntivitis en los ojos y fotodermatitis en la piel. Por estas razones, la irradiación UV-C requiere de precauciones de seguridad y no se puede utilizar para descontaminar áreas en presencia de humanos.
Las propiedades germicidas de la luz visible azul violeta (380-500 nm), especialmente dentro del rango de 405 a 450 nm, se han demostrado como una posible alternativa a la irradiación UV-C en escenarios de desinfección con presencia de humanos. Aunque se ha demostrado que 405 nm o longitudes de onda estrechamente relacionadas son menos germicidas que UVC, su potencial de inactivación se ha evaluado en bacterias patógenas como Listeria spp. y Clostridium spp. y en especies fúngicas como Saccharomyces spp. y Candida spp.
Se cree que el mecanismo subyacente de la inactivación mediada por la luz azul está asociado con la absorción de luz a través de fotosensibilizadores como las porfirinas, lo que resulta en la liberación de especies reactivas de oxígeno (ROS). La aparición de ROS se asocia con daños directos a biomoléculas como proteínas, lípidos y ácidos nucleicos, que son componentes esenciales de bacterias, hongos y virus. Asimismo, estos ROS también pueden conducir a la pérdida de permeabilidad de la membrana celular mediada por la oxidación lipídica.
Dada la falta de fotosensibilizadores endógenos como las porfirinas en los viriones (partículas víricas), se esperaba que la descontaminación eficiente de los virus (tanto envueltos como no envueltos) requerirá la adición de fotosensibilizadores exógenos.
Es por ello que los investigadores del Ichan School of Medicine at Mount Sinai se propusieron dar luz sobre este tema, centrando su investigación en la respuesta a tres preguntas claves: ¿la misma longitud de onda de luz de 405 nm que inactiva bacterias es capaz de inactivar virus envueltos? ¿Es un medio rico en porfirias necesario para esa inactivación)? ¿Se puede lograr esta inactivación utilizando niveles de irradiación seguros y comercialmente prácticos?
Sistema de desinfección con luz visible utilizado
Los investigadores utilizaron un sistemas de desinfección de luz visible disponible comercialmente, capaz de garantizar que la irradiancia utilizada sea segura y alcanzable en un entorno clínico.
En concreto, se trata de un downlight LED de 6’ disponible comercialmente para permitir su uso dentro de una campana de contención de nivel BSL-3. Dentro de la campana, la distancia entre la cara de la luminaria y la muestra fue de 10′′, mucho menos que los 1,5 m normales utilizados en aplicaciones normales de desinfección de toda la habitación. La salida de la luminarias se modificó electrónicamente durante su fabricación para que coincida con esta diferencia y garantizar que las mediciones representaran el rendimiento del dispositivo en uso real. En la siguiente figura se puede ver el dispositivo:

Como referencia, la cantidad de luz visible dentro del ancho de banda de 400-420 nm, medida en mW cm−2, es una medida de la «dosis» entregada al organismo objetivo y se utiliza para cuantificar esta relación similar a la utilizada en aplicaciones de desinfección UV.
Para examinar completamente este efecto, se utilizó una serie de valores de irradiancia que representan las condiciones reales de despliegue del producto en las habitaciones ocupadas. El valor más bajo (0,035 mW cm−2) representa una potencia monomodo y menor utilizada en aplicaciones de iluminación general, mientras que el valor más alto (0,6 mW cm−2) representa una potencia dual y de mayor potencia utilizada en aplicaciones de cuidados críticos como un quirófano.
Las muestras se irradiaron con los rangos de longitudes de onda representadas en la figura siguiente:
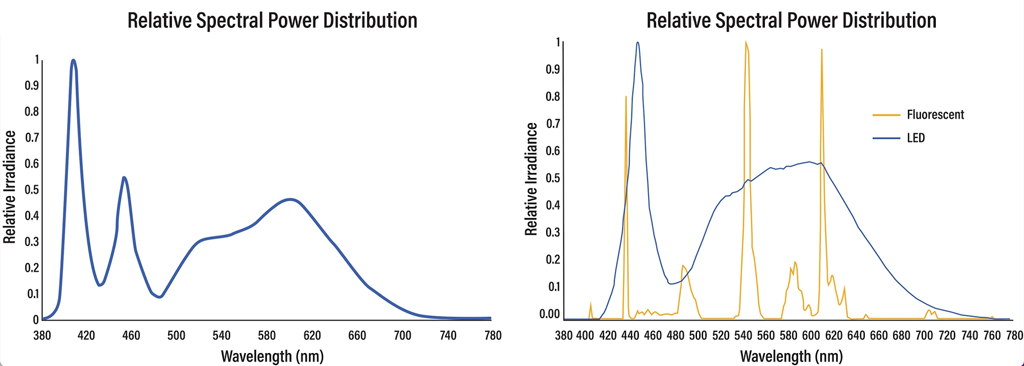
Esto se hizo deliberadamente por dos razones: (1) el trabajo previo había demostrado que la desinfección de la luz visible era principalmente activa a 405 nm y (2) para enfatizar la ciencia aplicada asociada con el uso clínico real, donde un virus en el medio ambiente podía exponerse tanto a 405 nm como a luz blanca regular en una habitación ocupada.
Las luces en el laboratorio BSL-3 eran fluorescentes tradicionales. Como se muestra en la Fig. 1B, los controles se expusieron solo a la iluminación fluorescente tradicional con una cantidad insignificante de luz desinfectante (< 0,001 mW cm−2) entre 400 y 420 nm. Debido a las diferencias inherentes entre la iluminación fluorescente y LED, los espectros LED estándar tienen una cantidad pequeña, pero medible, de luz desinfectante (0,006 mW cm−2) entre 400 y 420 nm. Como se mostrará más adelante, esta cantidad de luz puede tener un efecto desinfectante medible.
Resultados obtenidos
Inactivación del SARS-CoV-2 en ausencia de fotosensibilizadores
El SARS-CoV-2 es un virus envuelto en lípidos compuesto por un genoma de ARN y los resultados indican su susceptibilidad a la inactivación medida por la luz visible.
Sin el uso de fotosensibilizadores exógenos, los investigadore pudieron demostrar que la irradiación de luz visible de baja intensidad (0,035 mW cm−2) produjo una reducción de la inactivación del SARS-CoV-2 log10 0,3288 después de 4 h (0,5 J cm−2) y una inactivación total log10 1,0325 del SARS-CoV-2 después de 24 h (3,02 J cm−2).
Una dosis ligeramente más alta (0,076 mW cm−2) resultó en una reducción de log10 1.5393 después de 24 h (6,56 J cm−2), mientras que una dosis de irradiación de 0,150 mW cm−2 mostró un log de reducción de 10 2.0056 después de 24 h (12,96 J cm−2) de irradiación.
Finalmente, aumentar la dosis a 0,6 mW cm−2 produjo una reducción log10 2.3010 solo después de 8 h (17,28 J cm−2), lo que indica una inactivación de virus infecciosos dependientes del tiempo y la dosis.
Inactivación del virus de la gripe A
Para confirmar aún más estas observaciones, los investigadores utilizaron el virus de la gripe A, que es otro virus respiratorio humano con una envoltura lipídica y un genoma ARN segmentado.
Al irradiar durante 1 h a 0,6 mW cm−2 (2,16 J cm−2), se observó una reducción total de log10 0,1619 para el virus de la gripe A en comparación con la reducción de log10 0,4150 para SARS-CoV-2 en las mismas condiciones. Si bien ambos virus tienen envolturas lipídicas, hay claramente una diferencia aquí que requerirá más estudio.
Una posible explicación es la diferencia en el tamaño del virión que crea una sección transversal físicamente más pequeña para la absorción. (IAV ~ 120 nm y SARS-CoV-2 ~ 200 nm)- Sin embargo, ambos virus se desactivaron en gran medida después de 8 h logrando una reducción de más de 1,5 log10.
Inactivación de un virus de ARN no envuelto (EMCV)
Finalmente, los investigadores irradiaron un virus de ARN no envuelto, el virus de la encefalomiocarditis (EMCV).
Los resultados de investigaciones anteriores de la luz visible contra virus no envueltos demostraron la necesidad de fotosesibilizantes externos, como la saliva artificial, sangre, heces, etc. Sin un medio que contuviera porfirina, los investigadores esperaban poca o ninguna inactivación cuando este virus se irradiaba con luz visible.
Para estas mediciones, se utilizó la irradiancia más alta disponible de 0,6 mW cm−2. Como se anticipó, se observó solo una reducción log10 0.0969 después de 8 h, sin embargo, esto parece ser con la precisión estadística de la medición basada en los resultados obtenidos de irradiaciones más cortas (1, 2 y 4 h).
A modo de comparación, un estudio que involucró al virus M13-bacteriophage (un virus no envuelto) mostró una reducción de 3 log utilizando una irradiancia de 50 mW cm−2 (casi 100 veces mayor que la irradiancia más alta utilizada en este estudio) durante 10 h a 425 nm, apoyando aún más la idea de que los virus no envueltos pueden requerir dosis más altas de luz visible.
Potencial de desinfección de la iluminación LED
Las irradiaciones que utilizan iluminación LED estándar plantean algunas preguntas interesantes para su posterior discusión. Como se muestra en la figura anterior, la iluminación LED estándar (sin la adición específica de luz de 405 nm) tiene una cantidad pequeña pero medible de luz desinfectante (0,006 mW cm-2) en el rango de 400 nm a 420 nm. Esto es casi 6 veces la cantidad de luz desinfectante en comparación con la iluminación fluorescente tradicional, pero ⅙ de la cantidad más baja de 405 nm utilizada en el estudio.
Para cuantificar el efecto desinfectante de esta luz, se realizaron irradiaciones durante 4, 8, 12 y 24 horas. Los resultados muestran una reducción de 0,7 log a las 4 h en comparación con los controles. A las 24 h, se observó un total de 1,7 log utilizando una luz LED estándar . Ver figura 5
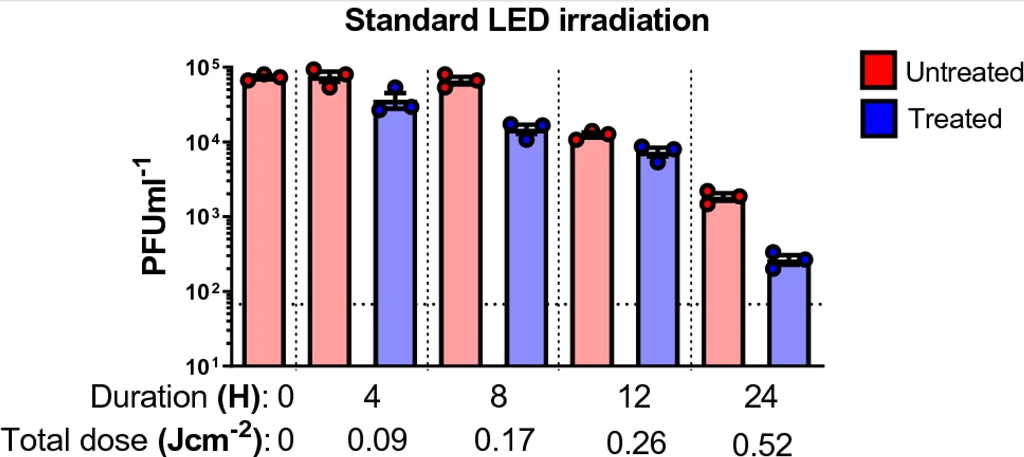
La magnitud de este efecto a menos de 24 h fue mayor de lo esperado según otras irradiaciones realizadas en este estudio. Los niveles intermedios de irradiación (4 h, 8 h y 12 h) fueron generalmente mayores de lo esperado, incluso teniendo en cuenta la incertidumbre experimental.
Un efecto similar fue observado por Bache, et al. en estudios de reducción de bacterias en toda la habitación. Observaron un efecto desinfectante para valores de irradiación tan bajos como 0,0023 mW cm-2. Este efecto se demostró que no estaba relacionado con el nivel de irradiación utilizado, lo que sugiere que la mera abundancia de luz de 405 nm puede iniciar la reacción química oxidante.
No obstante, nuestros resultados muestran claramente un efecto dependiente de la dosis. Una posible explicación de esta observación es que los niveles de irradiancia más bajos exponen a diferentes respuestas por parte de organismos específicos dentro de una población basada en la biología individual de ese organismo. Evidentemente, estos resultados sugieren que pueden intervenir otros factores y justifican una mayor investigación.
Conclusión
El estudio se llevó a cabo utilizando un medio líquido neutro compuesto por PBS sin ningún fotosensibilizador y los investigadores pudieron demostrar que luz visible puede inactiva virus envueltos lípidos, diferenciándose de la teoría que establece que los fotosensibilizadores son un requisito para la inactivación.
Los resultados obtenidos sugieren que el rendimiento de la luz visible contra el SARS-CoV-2 es similar a otros organismos que se encuentran comúnmente en el medio ambiente, como S. aureus. Estudios anteriores han demostrado que los niveles de irradiancia de luz visible utilizados en este estudio (0,035 mW cm−2 a 0,6 mW cm−2) reducen los niveles de bacterias en las habitaciones ocupadas y mejoran los resultados de los procedimientos quirúrgicos. Por lo tanto, es razonable concluir que la luz visible podría ser un desinfectante eficaz contra el SARS-CoV-2.
Más importante aún, esta desinfección puede funcionar continuamente, ya que es segura para los seres humanos según las pautas de exposición en la norma IEC 6247146. Esto significa que una vez que haya estado en uso durante un período de tiempo, el medio ambiente estará más limpio y seguro en todos los momentos futuros, incluso cuando esté ocupado por humanos.
Las irradiancias utilizadas en este estudio son muy bajas y podrían aplicarse fácilmente para desinfectar las áreas ocupadas de forma segura y continua dentro de hospitales, escuelas, restaurantes, oficinas y otros lugares.
Finalmente, los investigadores también quieren resaltar en sus conclusiones como es “de particular interés el potencial de la iluminación LED estándar para desempeñar un papel en la reducción de la presencia de SARS-CoV-2 en el medio ambiente”.
Artículo desarrollado a partir del paper: “The virucidal effects of 405 nm visible light on SARS-CoV-2 and influenza A virus” 2021. Autores: Raveen Rathnasinghe, Sonia Jangra, Lisa Miorin, Michael Schotsaert, Clifford Yahnke & Adolfo Garcίa-Sastre
Imagen de portada: Freepik