Una nueva técnica de foto-farmacología que utiliza la luz para activar los medicamentos de quimioterapia en células específicas se presenta como una forma prometedora de mejorar la eficacia de las terapias contra el cáncer, a la vez que previene efectos secundarios graves, según un estudio publicado el 9 de julio en la revista Cell.
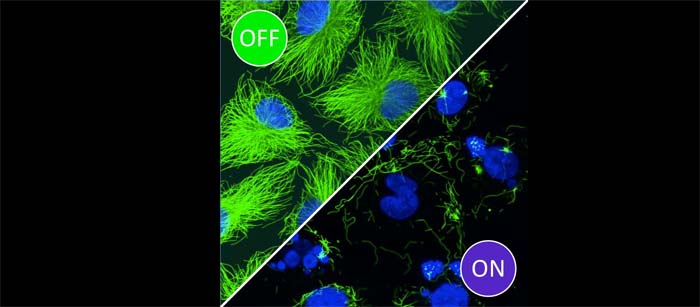
Foto de portada crédito: Malgorzata Borowiak, LMU Munich.
El enfoque denominado foto-farmacología podría ser utilizado para tratar una amplia gama de tumores con una precisión sin precedentes simplemente haciendo que los fármacos existentes contra el cáncer sean sensible a la luz – un enfoque que requiere menos tiempo y esfuerzo en comparación con los programas de investigación y demostración de fármacos tradicionales.
«Esperamos que nuestros compuestos sean utilizadas algún día en medicina para dar un golpe mortal a muchos tipos de tumores de cáncer localizados, sin producir efectos secundarios, lo que mejoraría los estándares de cuidados y también proporcionaría opciones de quimioterapia para los tumores que actualmente son intratables», dice el co-autor senior Oliver Thorn-Seshold de Ludwig-Maximilians-Universität München.
Algunos de los fármacos quimioterapéuticos más exitosos y ampliamente utilizados son los inhibidores que interfieren con la función de los microtúbulos – componentes del esqueleto de la célula que juegan un papel clave en la proliferación, la migración, y la supervivencia celular. Pero debido a que estos medicamentos no se dirigen específicamente a las células cancerosas, sino que también interfieren con la función de las células normales causan efectos secundarios graves, como daño al corazón y los nervios. Como resultado, los inhibidores de microtúbulos se limitan a menudo a dosis relativamente bajas que no proporcionan el mejor beneficio terapéutico.
Activar y desactivar el medicamento mediante luz
Para superar este reto, Thorn-Seshold y sus colaboradores desarrollaron un método para controlar ópticamente los fármacos inhibidores de microtúbulos actualmente en ensayos clínicos, con alta precisión espacial. La estrategia implica la identificación de un elemento estructural fijo requerido para la actividad biológica de un fármaco, a continuación, la sustitución de ese elemento con una bisagra flexible que se abre o cierra en respuesta a la luz azul.
«Entonces podemos utilizar la luz para activar o desactivar el medicamento, donde y cuando queramos, con la precisión de una célula individual», dice el co-autor Dirk Trauner, también de Ludwig-Maximilians-Universität München. «El resultado es que nuestros compuestos conservan los poderosos efectos contra el cáncer de inhibidores de microtúbulos existentes, pero añaden la bonificación de la localización específica de tejido.»

Dirigido solo a las células malignas
Los investigadores demostraron que estos compuestos modificados, llamados “ photostatins”, son eficaces en la inhibición de la proliferación y supervivencia de células a las que se dirige la luz, mientras que las células vecinas no se ven afectadas. Se pueden conectar y desconectar cientos de veces, haciéndolas adecuadas para aplicaciones a largo plazo tanto en la clínica y el laboratorio. Por otra parte, dado que se dirigen a una subunidad de microtúbulos crítico que se encuentra en las células de todas las plantas y animales, pueden ser utilizados para estudiar o tratar una amplia gama de organismos o procesos, incluso potencialmente una amplia gama de enfermedades en los seres humanos.
«Nos imaginamos que, ya que eliminan los efectos secundarios sistémicos, nuestros compuestos tienen potencial para ser utilizados en la medicina en dosis que son verdaderamente terapéuticas en tumores, logrando así una terapia mucho más eficaz que lo que es actualmente posible», dice Thorn-Seshold. «En el frente de la investigación, esperamos que permitan a los investigadores de todo el mundo desentrañar los detalles más finos que subyacen en muchos procesos biofísicos importantes en las células, por ejemplo, cómo se desarrolla la mitosis, cómo se se mueven o invaden las células, y cuán importante es la secuencia determinada genéticamente de la embriogénesis para el desarrollo correcto «.
Futuras aplicaciones con wearables
En futuros entornos clínicos, los autores del estudio se imaginan que los pacientes podrían usar diferentes wearables electrónicos como por ejemplo gafas azuladas para tratar el cáncer de ojo u otras enfermedades de los ojos, mientras que los individuos con cáncer de piel podrían usar un vendaje que proporcionase luz a los tumores. Por otro lado, los tumores internos podrían ser tratados con una red de pequeños LED implantables que parpadean cada pocos minutos para mantener el efecto quimioterapéutico sólo en el sitio en que está localizado el tumor.
Mientras tanto, los investigadores están tratando de superar los límites de su técnica con compuestos más precisos y eficaces, a la vez que perfeccionan la técnica para el tratamiento de tumores en ratones. «El campo de foto-farmacología es muy joven, así que puede llevar aun algún tiempo antes de que la industria farmacéutica reconozca el valor de estos compuestos», dice Thorn-Seshold. «Sin embargo, si nuestros estudios en curso tienen éxito, tendremos una propuesta convincente para un desarrollo preclínico más amplio, y estamos comprometidos a llegar tan lejos como podamos en la terapia real.»
###
Fuente Revista Cell, Borowiak et al «Photoswitchable Inhibitors of Microtubule Dynamics Optically Control Mitosis and Cell Death» http://dx.doi.org/10.1016/j.cell.2015.06.049